Bihar Board Class 11 Chemistry Solutions Chapter 8 अपचयोपचय अभिक्रियाएँ Textbook Questions and Answers, Additional Important Questions, Notes.
BSEB Bihar Board Class 11 Chemistry Solutions Chapter 8 अपचयोपचय अभिक्रियाएँ
Bihar Board Class 11 Chemistry अपचयोपचय अभिक्रियाएँ Text Book Questions and Answers
अभ्यास के प्रश्न एवं उनके उत्तर
प्रश्न 8.1
निम्नलिखित स्पीशीज में प्रत्येक रेखांकित तत्व की ऑक्सीकरण – संख्या का निर्धारण कीजिए –

उत्तर:
(क) माना NaH2PO4 में P की आ० सं० x है।
1 + 2 × 1 + x + 4 × (-2) = 0
1 + 2 + x – 8 = 0
या x – 5 = 0 या x = +5
(ख) माना NaHSO4 में S की आ० सं० x है।
1 + 1 + x4(-2) = 0
या x = + 6
(ग) माना N4P2O7 में P की आ० सं० x है।
4 × 1 + 2 × x + 7(-2) = 0
या 2x – 10 = 0
या x = +5
(घ) माना K2MNO4 में Mn की आ० सं० x है।
2 × 1 + x + 4(-2) = 0
या x – 6 = 0
या x = +6
(ङ) माना CaO2 में O की आ० सं० x है।
2 + 2x = 0
x = -1
(च) माना NaHB4 में S की आ० सं० x है।
1 + x + 4(-1) = 0
x = +3
2 × 1 + 2 × x + 7(-2) = 0
(छ) माना H2S2O7 में S की आ० सं० x है।
2 × 1 + 2 × x + 7(-2) = 0
या 2x – 12 = 0
या x = +6
(ज) माना KAI(SO4)2.12H2O में S की आ० सं० x
1 + 3 + 2(x – 8) + 12 × 2 + 12(-2) = 0
या 4 + 2x – 16 = 0
या x = +6
![]()
प्रश्न 8.2
निम्नलिखित यौगिकों के रेखांकित तत्वों की ऑक्सीकरण-संख्या क्या है तथा इन परिणामों को आप कैसे प्राप्त करते हैं?

उत्तर:
(क) माना KI3 में I की ऑक्सीकरण संख्या x है।
+ 1 + 3x = 0
या x = –\(\frac{1}{3}\)
(ख) माना H2S4O6 में माना S की ऑक्सीकरण संख्या x है।
या 2(+1) + 4x + 6(-2) = 0
4x – 10 = 0
या x = \(\frac{+5}{2}\) या 2.5
(ग) माना Fe3O4 में माना Fe की ऑक्सीकरण संख्या x है।
या 3x + 4(-2) = 0
3x – 8 = 0
या x = +\(\frac{8}{3}\)
(घ) माना CH3CH2OH में C की ऑक्सीकरण संख्या x है।
या x + 3(+1) + x + 2(+1) + 1(-2) + 1 = 0
x – 4 = 0
x = 2
(ङ) माना CH3COOH में C की ऑक्सीकरण संख्या x है।
या x + 3(+1) + x + (-2) + (-2) + 1 = 0
या 2x + 4 – 4 = 0
या x = 0
उपर्युक्त यौगिकों में निर्दिष्ट तत्व की ऑक्सीकरण संख्या भिन्नात्मक होती है। परन्तु हमें ज्ञात है कि भिन्नात्मक ऑक्सीकरण संख्या स्वीकार्य नहीं है; क्योकि इलेक्ट्रॉनों का सहभाजन अथवा स्थानान्तरण आंशिक नहीं हो सकता।
वास्तव में भिन्नात्मक ऑक्सीकरण अवस्था प्रेक्षित किए जा रहे तत्व की ऑक्सीकरण संख्याओं का औसत होता है तथा संरचना प्राचलों से ज्ञात होता है कि वह तत्व जिसकी भिन्नात्मक ऑक्सीकरण अवस्था होती है, अलग-अलग ऑक्सीकरण अवस्था में उपस्थित होता है। अतः उपर्युक्त ऑक्सीकरण संख्याओं से औसत ऑक्सीकरण अवस्थाएँ व्यक्त होती हैं।
![]()
प्रश्न 8.3
निम्नलिखित अभिक्रियाओं का अपचयोपचय अभिक्रियाओं के रूप में औचित्य स्थापित करने का प्रयास कीजिए –
(क) CuO(s) + H2(g) → Cu(s) + H2O(g)
(ख) Fe2O3(s) + 3CO(g) → 2Fe(s) + 3CO2(g)
(ग) 4BCl3(g) + 3 LiAIH4(s) → 2B2H6(g) + 3LiCl(s) + 3AlCl3(s)
(घ) 2K(s) + F2(g) → 2K+F–(s)
(ङ) 4NH3(g) + 5O2(g) → 4NO(g) + 6H2O(g)
उत्तर:
(क)

चूँकि यहाँ \(\mathrm{Cu}^{2+}\) की आ० सं० की +2 से 0 में कमी और H2 की आ० सं० की 0 से +1 तक वृद्धि हो रहीं, अतः \(\mathrm{Cu}^{2+}\) की Cu(s) में अपचयन तथा H2 का ऑक्सीकरण होता है।
अत: यह अभिक्रिया एक अपचयोपचय अभिक्रिया है।
(ख)

चूँकि यहाँ \(\mathrm{Fe}^{3+}\) का Fe(s) में अपचयन तथा C2+ का C4+ में ऑक्सीकरण हो रहा है; अत: यह एक अपचयोपचय अभिक्रिया है।

(ग)

चूँकि इस अभिक्रिया में आ० सं० में कोई परिवर्तन नहीं हो रहा है, अत: यह अपचयोपचय अभिक्रिया नहीं है।
(घ)

चूँकि यहाँ K(s) का K+ में ऑक्सीकरण और F2(g) का F– में अपचयन हो रहा है, अतः यह अभिक्रिया एक अपचयोपचय अभिक्रिया है।
(ङ)
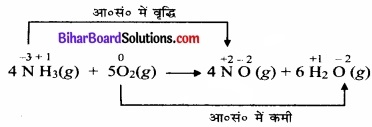
चूंकि इस अभिक्रिया में O2(g) का O2- में अपचयन और N3- का N+ में ऑक्सीकरण हो रहा है, अतः यह एक अपचयोपचय अभिक्रिया है।
![]()
प्रश्न 8.4
फ्लुओरीन बर्फ से अभिक्रिया करके यह परिवर्तन लाती है –
H2O(s) + F2(g) → HF(g) + HOF (g)
इस अभिक्रिया का अपचयोपचय औचित्य स्थापित कीजिए –
उत्तर:
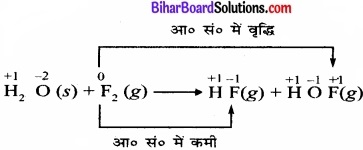
चूँकि फ्लुओरीन, ऑक्सीकरण तथा अपचयन दोनों प्रदर्शित करता है, अतः यह एक अपचयोपचय अभिक्रिया है।
प्रश्न 8.5
H2SO5, \(\mathrm{Cr}_{2} \mathrm{O}_{7}^{2-}\) तथा \(\mathrm{NO}^{3-}\) में सल्फर, क्रोमियम तथा नाइट्रोजन की ऑक्सीकरण संख्या की गणना कीजिए। साथ ही इन यौगिकों की संरचना बताइए तथा इसमें हेत्वाभास (fallacy) का स्पष्टीकरण दीजिए।
उत्तर:
H2SO5 में सल्फर की आ० सं० की गणना:
माना H2SO5 में S की आ० सं० x है।
2(+1) + x + 5(-2) = 0
x – 8 = 0
x = +8
यह ऑक्सीकरण संख्या ठीक नहीं है। चूंकि सल्फर की ऑक्सीकरण संख्या +6 से अधिक नहीं हो सकती। चूंकि H2SO5 में दो ऑक्सीजन परमाणु परॉक्साइड के रूप में होते हैं; अतः इनकी ऑक्सीकरण संख्या -1 होगी।
∴ 2(+1) + x + 3(-2) + 2(-1) = 0
2 + x – 6 – 2 = 0
x = 6
∴ H2SO5 की संरचना निम्नवत् है –
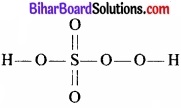
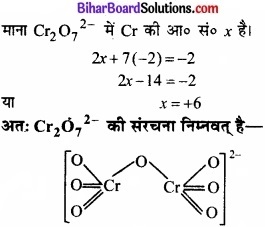
\(\mathrm{Cr}_{2} \mathrm{O}_{7}^{2-}\) में क्रोमियम की आ० सं० की गणना:
\(\mathrm{NO}^{3-}\) में नाइट्रोजन की आ० सं० की गणना:
माना \(\mathrm{NO}^{3-}\) में N की आ० सं० x है।
x + 3(-2) = -1
या x = +5
प्राप्त आ० सं० का मान सही है।
अत: \(\mathrm{NO}^{3-}\) की संरचना निम्नवत् है –

![]()
प्रश्न 8.6
निम्नलिखित यौगिकों के सूत्र लिखिए –
(क) मरक्यूरी (II) क्लोराइड
(ख) निकिल (II) सल्फेट
(ग) टिन (IV) ऑक्साइड
(घ) थैलियम (I) सल्फेट
(ङ) आयरन (III) सल्फेट
(च) क्रोमियम (II) ऑक्साइड
उत्तर:
(क) HgCl2
(ख) NiSO4
(ग) SnO2
(घ) TI2SO4
(ङ) Fe2(S4)3
(च) Cr2O3
प्रश्न 8.7
उन पदार्थों की सूची तैयार कीजिए, जिनमें कार्बन -4 से +4 तक की तथा नाइट्रोजन -3 से + 5 तक की ऑक्सीकरण अवस्था होती है।
उत्तर:
कार्बन की आ० सं० (-4 से +4 तक) वाले यौगिक निम्नवत् हैं –
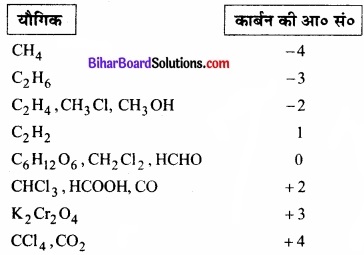
नाइट्रोजन की आ० सं० -3 से +3 तक वाले यौगिक निम्नवत् हैं –
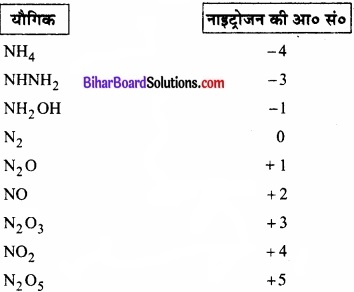
प्रश्न 8.8
अपनी अभिक्रियाओं में सल्फर डाइऑक्साइड तथा हाइड्रोजन परॉक्साइड ऑक्सीकारक तथा अपचायकदोनों ही रूपों में क्रिया करते हैं, जबकि ओजोन तथा नाइट्रिक अम्ल केवल ऑक्सीकारक के रूप में ही क्यों?
उत्तर:
सल्फर डाइऑक्साइड (SO2) तथा हाइड्रोजन परॉक्साइड (H2O2) में सल्फर तथा ऑक्सीजन की ऑक्सीकरण अवस्थाएँ क्रमश: +4 तथा -1 हैं। चूँकि इन यौगिकों की रासायनिक अभिक्रियाओं में ऑक्सीकरण में वृद्धि या कमी हो सकती है, अतः ये ऑक्सीकारक तथा अपचायक दो रूपों में कार्य करते हैं।
उदाहरणार्थ –

ओजोन (O3) में ऑक्सीजन की ऑक्सीकरण अवस्था शून्य है तथा नाइट्रिक अम्ल में नाइट्रोजन की ऑक्सीकरण अवस्था +5 है। चूँकि ये दोनों आ० सं० में कमी तो प्रदर्शित करते हैं, परन्तु वृद्धि नहीं करते, अत: ये केवल ऑक्सीकारक की भाँति कार्य करते हैं, अपचायक के रूप में नहीं।
![]()
प्रश्न 8.9
इन अभिक्रिया को देखिए –
(क) 6CO2(g) + 6H2O(l) → C6H12O6(aq) + 6O2(g)
(ख) O3(g) + H2O2 → H2O(l) + 2O2(g)
बताइए कि इन्हें निम्नलिखित ढंग से लिखना ज्यादा उचित क्यों है?
(क) 6CO2(g) + 12H2O(l) → C6H12O6(aq) + 6H2O(l) + 6O2(g)
(ख) O3(g) + H2O2(l) → H2O(l) + O2(g) + O2(g)
उपरोक्त अपचयोपचय अभिक्रियाओं (क) तथा (ख) के अन्वेषण की विधि सुझाइए।
उत्तर:
(क) 6CO2(g) + 6H2O(l) → C6H12O6(aq) + 6O2(g)
इस समीकरण को आयन-इलेक्ट्रॉन विधि द्वारा सन्तुलित करते हैं –
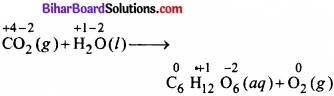
ऑक्सीकरण तथा अपचयन अर्द्ध-अभिक्रियाएँ लिखने पर,

ऑक्सीकरण अर्द्ध-अभिक्रिया को सन्तुलित करने पर,

उपर्युक्त दोनों सन्तुलित अर्द्ध-अभिक्रियाएँ जोड़ने पर,

यह अभिक्रिया के अन्वेषण की विधि सुझाता है अर्थात् किस प्रकार इलेक्ट्रॉन त्यागे अथवा ग्रहण किया जाते हैं। इसके साथ-साथ अभिक्रिया को उपर्युक्त संशोधित रूप में लिखने का उचित कारण स्पष्ट करता है।
(ख) O3(g) + H2O2(l) → H2O(l) + 2O2(g)
इस समीकरण को आयन-इलेक्ट्रॉन विधि द्वारा सन्तुलित करते हैं –

सन्तुलित ऑक्सीकरण तथा अपचयन अर्द्ध-अभिक्रियाएँ लिखकर उन्हें जोड़ने पर,
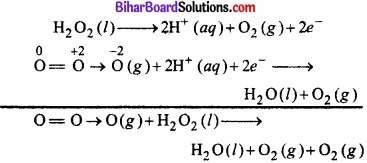
* इस अभिक्रिया में O3 ऑक्सीकारक की भाँति तथा H2O2 अपचायक की भाँति कार्य करते हैं।
* यदि दो समान परमाणुओं के मध्य एक उपसहसंयोजी आबन्ध उपस्थित होता है तो दाता परमाणु +2 ऑक्सीकरण संख्या प्राप्त करता है तथा ग्राही -2 ऑक्सीकरण संख्या प्राप्त करता है। इस प्रकार अभिक्रिया के अन्वेषण की विधि स्पष्ट हो जाती है तथा इसे संशोधित रूप में लिखने का कारण भी स्पष्ट हो जाता है।
![]()
प्रश्न 8.10
AgF2 एक अस्थिर यौगिक है। यदि यह बन जाए तो यह यौगिक एक अतिशक्तिशाली ऑक्सीकारक की भाँति कार्य करता है? क्यों?
उत्तर:
AgF2 वियोजित होकर Ag+ तथा 2F– देता है।
Ag2+ एक इलेक्ट्रॉन ग्रहण करके Ag+ में अपचयित हो जाता हैं –
Ag2+ + e– → Ag+
Ag+ का इलेक्ट्रॉनिक विन्यास निम्नवत् है –
1s2, 2s22p6, 3s2 3p6 3d10, 4s2 4p6 4d10
चूंकि यह इलेक्ट्रॉनिक विन्यास d – कक्षकों के पूर्णतया भरे होने के स्थाई है, अत: AgF2 एक अतिशक्तिशाली ऑक्सीकारक की भाँति कार्य करता है।
प्रश्न 8.11
“जब भी एक ऑक्सीकारक तथा अपचायक के बीच अभिक्रिया सम्पन्न की जाती है, तब अपचायक के आधिक्य में निम्नतर ऑक्सीकरण अवस्था का यौगिक तथा ऑक्सीकारक के आधिक्य में उच्चतर ऑक्सीकरण अवस्था का यौगिक बनता है।” इस वक्तव्य का औचित्य तीन उदाहरण देकर दीजिए।
उत्तर:
1. Fe तथा O2 के मध्य अभिक्रिया –

2. Fe तथा Cl2 के मध्य अभिक्रिया –

3. NH3 तथा Cl2 के मध्य अभिक्रिया –

प्रश्न 8.12
इन प्रेक्षणों की अनुकूलता को कैसे समझाएँगे?
(क) यद्यपि क्षारीय पोटेशियम परमैंगनेट तथा अम्लीय पोटैशियम परमैंगनेट दोनों ही ऑक्सीकारक हैं। फिर भी टॉलूईन से बेन्जोइक अम्ल बनाने के लिए हम ऐकोहॉलिक पोटैशियम परमैंगनेट का प्रयोग ऑक्सीकारक के रूप में क्यों करते हैं? इस अभिक्रिया के लिए सन्तुलित अपचयोपचय समीकरण दीजिए।
(ख) क्लोराइडयुक्त अकार्बनिक यौगिक में सान्द्र सल्फ्यूरिक अम्ल डालने पर हमें तीक्ष्ण गन्ध वाली HCl गैस प्राप्त होती है, परन्तु यदि मिश्रण में ब्रोमाइड उपस्थिति हो तो हमें ब्रोमीन की लाल वाष्प प्राप्त होती है, क्यों?
उत्तर:
(क) उदासीन माध्यम में KMnO4 निम्नलिखित प्रकार से ऑक्सीकारक की भाँति कार्य करता है –
Mn\(\mathrm{O}^{4-}\) + 2H2O + 3e2- → MnO2 + 4OH–
प्रयोगशाला में टॉलूईन को बेन्जोइक अम्ल में ऑक्सीकृत करने के लिए क्षारीय KMnO4 का प्रयोग किया जाता है –

औद्योगिक निर्माण के दौरान ऐल्कोहॉलिक KMnO4 को प्रयोग करने के निम्नलिखित दो कारण हैं –
1. अभिक्रिया के दौरान क्षार (OH– आयन) स्वत: उत्पन्न हो जाता है; अतः क्षार मिलाने का अतिरिक्त व्यय नहीं होता।
2. एक कार्बनिक ध्रुवी विलायक, एथिल ऐल्कोहॉल, दोनों अभिकारकों, KMnO4 (इसकी ध्रुवी प्रकृति के कारण) तथा टॉलूईन (इसके कार्बनिक यौगिक होने के कारण) का मिक्षित करने में सहायता प्रदान करता है।
(ख) एक क्लोराइडयुक्त अकार्बनिक यौगिक; जैसे –
NaCl, जब सान्द्र सल्फ्यूरिक अम्ल के साथ अभिक्रिया करता है, तब हाइड्रोजन क्लोराइड गैस उत्पन्न होती है।
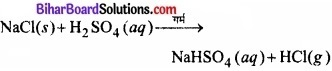
ब्रोमाइड (जैसे – NaBr) की H2SO4 से अभिक्रिया पर भी HBr की वाष्प उत्पन्न होती हैं, परन्तु HBr के प्रबल अपचायक होने के कारण, यह सल्फ्यूरिक अम्ल द्वारा ऑक्सीकृत होकर ब्रोमीन की लाल वाष्प मुक्त करता है।
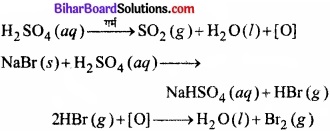
![]()
प्रश्न 8.13
निम्नलिखित अभिक्रियाओं में ऑक्सीकृत, अपचयित, ऑक्सीकारक तथा अपचायक पदार्थ पहचानिए –

उत्तर:

प्रश्न 8.14
निम्नलिखित अभिक्रियाओं में एक ही अपचायक थायोसल्फेट, आयोडीन तथा ब्रोमीन से अलग-अलग प्रकार से अभिक्रिया क्यों करता है?
\(2 \mathrm{S}_{2} \mathrm{O}_{3}^{2-}\) (aq) + I2(s) → \(2 \mathrm{S}_{4} \mathrm{O}_{6}^{2-}\) (aq) + 2I– (aq)
\(\mathbf{s}_{2} \mathbf{o}_{3}^{2-}\) (aq) + 2Br2(l) + 5H2O(l) → \(2 \mathrm{S}_{2} \mathrm{O}_{4}^{2-}\) (aq) + 4Br– (aq) + 10H+ (aq)
उत्तर:
चूँकि \(2 \mathrm{S}_{2} \mathrm{O}_{3}^{2-}\) में S की ऑक्सीकरण संख्या +2 से \(2 \mathrm{S}_{4} \mathrm{O}_{6}^{2-}\) आयन में S की ऑक्सीकरण संख्या +\(\frac{5}{2}\) में परिवर्तित हो जाती है, अत: आयोडीन थायोसल्फेट आयन को टेट्राथायेनेट आयन में ऑक्सीकृत कर देती है –
चूँकि S की ऑक्सीकरण संख्या +2(\(2 \mathrm{S}_{2} \mathrm{O}_{3}^{2-}\) में) से +6(\(\mathrm{SP}_{4}^{2-}\) आयन में) परिवर्तित हो जाती है, अत: ब्रोमीन (Br2) थायोसल्फेट आयन को सल्फेट आयन में ऑक्सीकृत कर देती है।
अतः ब्रोमीन, आयोडीन की तुलना में प्रबल ऑक्सीकारक है –
(E0Br2/2\(\overrightarrow{\mathrm{Br}}\) = 1.09V तथा E0I2/2I– = 0.54V)
प्रश्न 8.15
अभिक्रिया देते हुए सिद्ध कीजिए कि हैलोजनों में फ्लुओरीन श्रेष्ठ ऑक्सीकारक तथा हाइड्रोहैलिक ‘यौगिकों में हाइड्रोआयोडिक अम्ल श्रेष्ठ अपचायक है।
उत्तर:
हैलोजेनों की इलेक्ट्रॉन ग्रहण करने की प्रवृत्ति प्रबल होती है। अतः ये शक्तिशाली ऑक्सीकारक होते हैं। हैलोजेनों की ऑक्सीकारक क्षमता का आपेक्षिक क्रम निम्नलिखित है –

हैलोजेनों में फ्लुओरीन श्रेष्ठ ऑक्सीकारक है, इस तथ्य की पुष्टि इस प्रकार हो सकता है कि यह अन्य हैलोजेनों को उनके यौगिकों से मुक्त कर देता है। उदाहरणार्थ –
2KCl + F2 → 2KF + Cl2↑
2KBr + F2 → 2KF + Br2↑
2KI + F2 → 2KF + I2↑
हाइड्रोहैलिक अम्लों में हाइड्रोआयोडिक अम्ल श्रेष्ठ अपचायक है; क्योंकि इसकी आबन्ध वियोजन एन्थैल्पी न्यूनतम (299kJmol-1) होती है।

मेथेन का आयोडीनीकरण (iodination) उत्क्रमणीय प्रकृति का होता है; क्योंकि अभिक्रिया में उत्पन्न HI, प्रबलतम अपचायक होने के कारण आयोडो-मेथेन को पुनः मेथेन में परिवर्तित कर देता है।
या CH4 + I2 → CH3I + HI
CH3 + HI → CH4 + I2
CH4 + I2 ⇄ CH2I + HI
![]()
प्रश्न 8.16
निम्नलिखित अभिक्रिया क्यों होती है?
\(\mathrm{XeO}_{6}^{4-}\) (aq) + 2F– (aq) + 6H+ (aq) → XeO3(g) + F2(g) + 3H2O(l)
यौगिक Na4XeO6 (जिसका एक भाग \(\mathrm{XeO}_{6}^{4-}\) है) के बारे में आप इस अभिक्रिया में क्या निष्कर्ष निकाल सकते है।
उत्तर:
\(\mathrm{XeO}_{6}^{4-}\) (aq) + 2F– (aq) + 6H+ (aq) → XeO3(g) + F2(g) + 3H2O(l)
यह अभिक्रिया F2 के रासायनिक विधियों द्वारा निर्माण की हाल ही में विकसित की गई रासायिकन विधियों की श्रेणी में से एक है। यह प्रचलित विद्युत-रासायनिक विधि नहीं है। इस अभिक्रिया में \(\mathrm{XeO}_{6}^{4-}\) एक प्रबल ऑक्सीकरण के रूप में कार्य करते हुए F– को F2 में ऑक्सीकृत कर देता है जो विद्युत-रासायनिक श्रेणी में सर्वाधिक अपचायक क्षमता वाला तत्व है।
F2 के निर्माण की एक अन्य रासायनिक विधि में अन्य प्रबल ऑक्सीकारक K2MnF6 प्रयुक्त होता है –
2K2MDF6 + 4SbF5 → 4KSbF6 + 2MnF3 + F2 ↑
प्रश्न 8.17
निम्नलिखित अभिक्रियाओं में –

उत्तर:
(क) Ag+ आयन Ag में अपचयित हो अवक्षेपित हो जाते हैं।
(ख) Cu2+ आयन Cu में अपचयित हो जाता हैं अवक्षेपित हो जाता है।
(ग) संकर में उपस्थित Ag+ (aq).Ag में अपचयित हो जाते हैं जो अवक्षेपित हो जाता है।
(घ) Cu2+ (aq) आयतन (CH6H5OCHO) द्वारा अपचयित नहीं होते एक दुर्बल अपचायक है।
प्रश्न 8.18
आयन-इलेक्ट्रॉन विधि द्वारा निम्नलिखित रेडॉक्स अभिक्रियाओं को सन्तुलित कीजिए –

उत्तर:
(क) दी हुई अभिक्रिया है –
\(\mathrm{MnO}_{4}^{-}\) (aq) + I– (aq) → MnO2(s) + I2(s)
पद 1.
दो अर्द्ध-अभिक्रियाएँ निम्नवत् हैं –
1. ऑक्सीकरण अर्द्ध-अभिक्रिया:
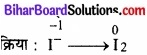
2. अपचयन अर्द्ध-अभिक्रिया:
![]()
पद 2.
ऑक्सीकरण अर्द्ध-अभिक्रिया में I परमाणु का सन्तुलन करने पर इस प्रकार लिखते हैं –
2I– (aq) → I2(s)
पद 3.
O परमाणुओं के सनतुलन करने के लिए अपचयन अभिक्रिया में दाईं ओर 2 जल-अणु जोड़ते हैं –
\(\mathrm{MnO}_{4}^{-}\) (aq) → MnO2(s) + 2H2O(l)
H परमाणुओं के सन्तुलन के लिए बाईं ओर चार H+ आयन जोड़ते हैं –
\(\mathrm{MnO}_{4}^{-}\) (aq) + 4H+ (aq) → MnO2 (s) + 2H2O(l)
चूँकि अभिक्रिया क्षारीय माध्यम में होती है, अत: 4H+ के लिए समीकरण के दोनों ओर हम 4OH– जोड़ देते हैं।
\(\mathrm{MnO}_{4}^{-}\) (aq) + 4H+ (aq) + OH– (aq) → MnO2 (s) 2H2O(l) + 4H– (aq)
H+ तथा OH– आयनों के योग को H2O से बदलने पर परिणामी समीकरण इस प्रकार है –
\(\mathrm{MnO}_{4}^{-}\) (aq) + 2H2O(l) + 3e– → MnO2 (s) + 4OH– (aq)
पद 5.
दोनों अभिक्रियाओं के आवेशों द्वारा संतुलित करते हैं जिसे निम्न प्रकार से दर्शाया गया है –
2I– (a) → I2 (s) + 2e–
\(\mathrm{MnO}_{4}^{-}\) (aq) + 2H2O(l) + 3e– → MnO2 (s) + 4OH– (aq)
अब दोनों इलेक्ट्रॉनों की संख्या को बराबर करने के लिए ऑक्सीकरण अर्द्ध-अभिक्रिया को 3 से तथा अपचयन अर्द्ध अभक्रिया को 2 से गुणा करके जोड़ने पर –
6l– (aq) + \(\mathrm{2MnO}_{4}^{-}\) (aq) + 4H2O(l) → 3l2 (s) + 2MnO2 (s) + 8OH– (aq) जो कि अभीष्ट संतुलित समीकरण है।
(ख) दी हुई अभिक्रिया है –
\(\mathrm{MnO}_{4}^{-}\) (aq) + 2SO2 (g) → Mn2+ (aq) + \(\mathrm{HSO}_{4}^{-}\) (aq)
पद 1.
दो अर्द्ध-अभिक्रियाएँ निम्नवत् हैं –
1. ऑक्सीकरण अर्द्ध-अभिक्रिया:

2. अपचयन अर्द्ध-अभिक्रिया:

पद 2.
ऑक्सीजन परमाणु के सन्तुलन के लिए अर्द्ध ऑक्सीकरण अभिक्रिया (i) में बाईं ओ 2 जल अणु जोड़ने पर –
SO2 (g) + 2H2O(l) → \(\mathrm{HSO}_{4}^{-}\) (aq)
हाइड्रोजन परमाणुओं के सन्तुलन के लिए ऑक्सीकरण अभिक्रिया (ii) में दाईं ओर 3H+ आयन जोड़ने पर
SO2 (g) + 2H2O(l) → \(\mathrm{HSO}_{4}^{-}\) (aq) + 3H+ (aq)
पद 3.
ऑक्सीजन परमाणुओं के सन्तुलन के लिए अपचयन अभिक्रिया के दाईं ओर चार जल-अणु जोड़ने पर –
\(\mathrm{MnO}_{4}^{-}\) (aq) → Mn2+ (aq) + 4H2O(l)
हाइड्रोजन परमाणुओं के सन्तुलन के लिए अपचयन अर्द्ध-अभिक्रिया के बाईं ओर 8H+ आयन जोड़ने पर –
\(\mathrm{MnO}_{4}^{-}\) (aq) + 8H+ (aq) → Mn2+ (aq) + 4H2O(l)
पद 4.
दोनों अर्द्ध-अभिक्रियाओं में आवेशों का संतुलन इलेक्ट्रॉनों द्वारा करते हैं –
SO2 (g) + 2H2O(l) → \(\mathrm{HSO}_{4}^{-}\) (aq) + 3H+ (aq) + 2e–
\(\mathrm{MnO}_{4}^{-}\) (aq) + 8H+ (aq) + 5e– → Mn2+ (aq) + 4H2O(l)
दोनों इलेक्ट्रॉनों की संख्या एकसमान बनाने के लिए ऑक्सीकरण अर्द्ध-अभिक्रिया को 5 से तथा अपचयन अर्द्धअभिक्रिया को 2 से गुणा करके जोड़ने पर –
\(\mathrm{2MnO}_{4}^{-}\) (aq) + 5SO2 (g) + 2H2O (l) + H+ (aq) → 5\(\mathrm{HSO}_{4}^{-}\) (aq) + 2Mn2+ (aq) जो अभीष्ट संतुलित समीकरण है।
(ग)
पद 1. पहले हम ढाँचा समीकरण लिखते हैं –
H2O2 (aq) + Fe2+ (aq) → Fe3+ (aq) + H2O (l)
पद 2.
दो अर्द्ध-अभिक्रियाएँ इस प्रकार हैं –
1. ऑक्सीकरण अर्द्ध-अभिक्रिया:

2. अपचयन अर्द्ध-अभिक्रिया:
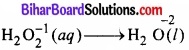
पद 3.
ऑक्सीकरण अर्द्ध-अभिक्रिया में Fe परमाणु का सन्तुलन करने पर हम लिखते हैं –
Fe2+ (aq) → Fe3+ (aq)
पद 4.
अपचयन अर्द्ध-अभिक्रिया में O परमाणुओं के सन्तुलन के लिए हम समीकरणं को इस प्रकार लिखते हैं –
H2O2 (aq) → 2H2O (l)
H परमाणुओं के सन्तुलन के लिए हम बाईं ओर दो H+ आयन जोड़ देते हैं –
H2O2 (aq) + 2H+ (aq) → 2H2O (l)
पद 5.
इस पद में हम दोनों अर्द्ध-अभिक्रियाओं में आवेश का सन्तुलन दर्शाई गई विधि द्वारा करते हैं –

इलेक्ट्रॉन की संख्या को एकसमान बनाने के लिए ऑक्सीकरण अर्द्ध-अभिक्रिया को 2 से गुणा करते हैं –
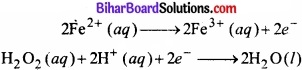
पद 6.
दोनों अर्द्ध-अभिक्रियाओं को जोड़ने पर –
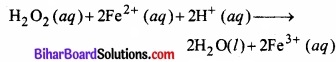
अन्तिम अत्यापन दर्शाता है कि दोनों ओर के परमाणुओं की संख्या तथा आवेश की दृष्टि से समीकरण सन्तुलित है।
(घ)
पद 1.
पहले हम ढाँचा समीकरण लिखते हैं –
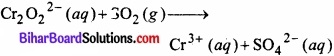
पद 2.
दो अर्द्ध-अभिक्रियाएँ इस प्रकार हैं –
1. ऑक्सीकरण अर्द्ध-अभिक्रिया:

2. अपचयन अर्द्ध-अभिक्रिया:

पद 3.
ऑक्सीकरण अर्द्ध-अभिक्रिया में O परमाणओं के सन्तुलन के लिए हम बाईं ओर दो जल अणु जोड़ते हैं –
![]()
H परमाणुओं के सन्तुलन के लिए हम दाईं ओर 4H+ आयन जोड़ देते हैं –
![]()
पद 4.
अपचयन अर्द्ध-अभिक्रिया में O परमाणुओं के सन्तुलन के लिए हम दाईं ओर सात जल अणु जोड़ते हैं तथा Cr परमाणु को भी सन्तुलित करते हैं –
![]()
H परमाणु के सन्तुलन के लिए हम बाईं ओर चौदह H+ आयन जोड़ देते हैं –

पद 5.
इस पद में हम दोनों अर्द्ध-अभिक्रियाओं में आवेश का सन्तुलन इस प्रकार करते हैं –

पद 6.
दोनों अर्द्ध-अभिक्रियाओं को जोड़ने पर –
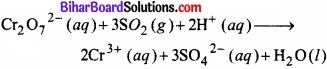
अन्तिम सत्यापन दर्शाता है कि दोनों ओर के परमाणुओं की संख्या तथा आवेश की दृष्टि से समीकरण सन्तुलित है।
![]()
प्रश्न 8.19
निम्नलिखित अभिक्रियाओं के समीकरणों को आयन-इलेक्ट्रॉन तथा ऑक्सीकरण संख्या विधि (क्षारीय माध्यम में) द्वारा सन्तुलित कीजिए तथा इनमें ऑक्सीकरण और अपचायकों की पहचान कीजिए –

उत्तर:
(क) आयन इलेक्ट्रॉन विधि से समीकरण सन्तुलित करना –
पद 1.
पहले ढाँचा समीकरण लिखते हैं –
![]()
पद 2.
दो अर्द्ध-अभिक्रियाएँ इस प्रकार हैं –
1. ऑक्सीकरण अर्द्ध-अभिक्रिया:

2. अपचयन अर्द्ध-अभिक्रिया:

P ऑक्सीकारक अपचायक दोनों की भाँति कार्य करता
पद 3.
ऑक्सीकरण अर्द्ध-अभिक्रिया में पहले P परमाणुओं को सन्तुलित करके O परमाणुओं के सन्तुलन के लिए हम बाई ओर आठ जल अणु जोड़ते हैं।
![]()
इस अभिक्रिया में H– परमाणु सन्तुलित करने के लिए आठ H+ आयन दाईं ओर जोड़ते हैं।

अब चूँकि अभिक्रिया क्षारीय माध्यम में होती है; अत: दोनों ओर OH– आयन जोड़ते हैं –

पद 4.
अपचयन अर्द्ध-अभिक्रिया में P परमाणुओं को सन्तुलित करते हैं –
P4 → 4PH3 (g)
H– परमाणुओं के सन्तुलन के लिए हम उपर्युक्त अभिक्रिया में बाईं ओर बारह H+ आयन जोड़ देते हैं –
P4 (s) + 12H+ (aq) → 4PH3 (g)
क्योंकि अभिक्रिया क्षारीय माध्यम में होती है; अत: 12H+ आयनों के लिए 12OH– आयन समीकरण के दोनों ओर जोड़ते –

H+ तथा OH+ के संयोग से जल अणु बनाने के कारण परिणामी समीकरण निम्नलिखित प्रकार से होगी –
P4 (s) + 12H2O (l) → 4PH3 (g) + 12OH– (aq)
पद 5.
इस पद में हम दोनों अर्द्ध-अभिक्रियाओं में आवेश का सन्तुलन निम्नवत् करते हैं –

पद 6.
उपर्युक्त दोनों अर्द्ध-अभिक्रियाओं को जोड़ने पर –

अन्तिम सत्यापन दर्शाता है कि समीकरण में दोनों ओर के परमाणुओं की संख्या तथा आवेश की दृष्टि से समीकरण सन्तुलित है।
ऑक्सीकरण संख्या विधि से समीकरण सन्तुलित करना –
पद 1.
अभिक्रिया का ढाँचा इस प्रकार है –
P4 (s) + OH– (aq) → PH3 (g) + H2PO2– (aq)
पद 2.
अभिक्रिया में P की ऑक्सीकरण संख्या लिखते हैं –

यह इस बात का सूचक है कि P ऑक्सीकारक तथा अपचायक दोनों रूपों में कार्य करता है।
पद 3.
P की ऑक्सीकरण अवस्था 3 घटती है तथा 1 बढ़ती है। अतः हमें H2PO2– की गुणा 3 से करनी होगी।
P4 (s) + OH– (aq) → PH3 (g) + 3H2PO2– (aq)
पद 4.
चूँकि अभिक्रिया क्षारीय माध्यम में हो रही है तथा दोनों ओर के आयनों का आवेश एकसमान नहीं है। अत: हम बाई ओर दो OH– आयन जोड़ेंगे जिससे आवेश एकसमान हो जाए।
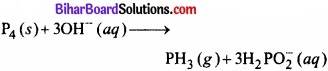
पद 5.
इस पद में हाइड्रोजन आयनों को सन्तुलित करने के लिए हम तीन जल अणुओं को बाईं ओर जोड़ते हैं –

(ख) आयन-इलेक्ट्रॉन विधि से समीकरण सन्तुलित करना –
पद 1.
पहले ढाँचा समीकरण लिखते हैं –
N2H4 (l) + ClO3– (aq) → NO(g) + Cl– (g)
पद 2.
दो अर्द्ध-अभिक्रियाएँ इस प्रकार हैं –
1. ऑक्सीकरण अर्द्ध-अभिक्रिया:
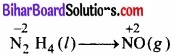
2. अपचयन अर्द्ध-अभिक्रिया:

(N2H4 अपचायक तथा ClO3– ऑक्सीकारक की भाँति कार्य करता है।)
पद 3.
ऑक्सीकरण अर्द्ध-अभिक्रिया में N – परमाणुओं को सन्तुलित करते हैं –
N2H4(l) → 2NO(g)
अब O परमाणुओं को सन्तुलित करने के लिए समीकरण में बाईं ओर दो जल अणु जोड़ते हैं –
N2H4(l) + 2H2O(l) → 2NO(g)
अब H परमाणुओं को सन्तुलित करने के लिए समीकरण में दाईं ओर 8H+ जोड़ते हैं –
N2H4(l) + 2H2O(l) → 2NO(g) + 8H+(aq)
चूँकि अभिक्रिया क्षारीय माध्यम में हो रही है; अतः समीकरण के दोनों ओर 8OH– आयन जोड़ते हैं –
N2H4(l) + 8OH–(aq) → 2NO(g) + 8H+ + 8OH–(aq)
H+ तथा OH+ आयनों के संयोग पर जल अणु बनने के कारण समीकरण निम्नवत होगी –
N2H4(l) + 8OH–(aq) → 2NO(g) + 6H2O(aq)
पद 4.
अपचयन अर्द्ध-अभिक्रिया में O परमाणुओं के सन्तुलन के लिए समीकरण के दाईं ओर तीन जल अणु जोड़ते हैं –
ClO3– (aq) → Cl– (g) + 3H2O(l)
H– परमाणुओं को सन्तुलित करने के लिए समीकरण के बाईं ओर छह H+ आयन जोड़ते हैं –
ClO3– (aq) + 6H+ (aq) → Cl– (g) + 3H2O(l)
चूँकि अभिक्रिया क्षारीय माध्यम में होती है; अतः समीकरण में दोनों ओर छह OH– आयन जोड़ते हैं –

पद 5.
इस पद में हम दोनों अर्द्ध-अभिक्रियाओं के आवेश का सन्तुलन निम्नवत् करते हैं –

इलेक्ट्रॉनों की संख्या समान करने के लिए ऑक्सीकरण अर्द्ध-अभिक्रिया को 3 से तथा अपचयन अर्द्ध-अभिक्रिया को 4 से गुणा करते हैं –
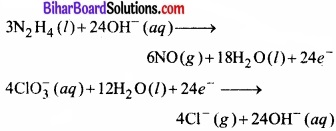
पद 6.
दोनों अर्द्ध-अभिक्रियाओं को जोड़ने पर –
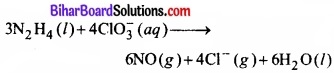
अन्तिम सत्यापन दर्शाता है कि उपर्युक्त समीकरण परमाणुओं की संख्या तथा आवेश की दृष्टि से सन्तुलित है।
ऑक्सीकरण संख्या विधि से समीकरण सन्तुलित करना –
पद 1.
अभिक्रिया का ढाँचा इस प्रकार है –
N2H4(l) + ClO3– (aq) → NO(g) + Cl– (g)
पद 2.
अभिक्रिया में N तथा Cl की ऑक्सीकरण संख्या लिखते हैं –

स्पष्ट है कि N2H4 अपचायक तथा ClO3– ऑक्सीकारक के रूप में कार्य करते हैं।
पद 3.
ऑक्सीकरण संख्या में होने वाली वृद्धि तथा कमी की गणना करते हैं तथा इन्हें एकसमान बनाते हैं।

पद 4.
चूँकि अभिक्रिया क्षारीय माध्यम में हो रही है तथा अभिक्रिया आवेश की दृष्टि से सन्तुलित है; अतः O तथा H परमाणु के सन्तुलन के लिए अभिक्रिया में दाईं ओर 6 जल अणु जोड़ देने पर पूर्णतया सन्तुलित समीकरण प्राप्त हो जाएगी।
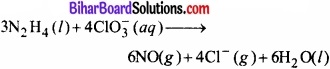
यह सन्तुलित समीकरण है।
(ग) आयन-इलेक्ट्रॉन विधि से समीकरण सन्तुलित करना –
पद 1.
पहले ढाँचा समीकरण लिखते हैं –

पद 2.
दो अर्द्ध-अभिक्रियाएँ इस प्रकार हैं –
1. ऑक्सीकरण अर्द्ध-अभिक्रिया:
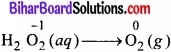
2. अपचयन अर्द्ध-अभिक्रिया:
![]()
(H2O2 आपचायक तथा Cl2O7 ऑक्सीकारक की भाँति कार्य करते हैं।)
पद 3.
ऑक्सीकरण अर्द्ध-अभिक्रिया में H परमाणुओं के सन्तुलन के लिए हम दो H+ दाईं ओर जोड़ते हैं –
H2O2 (aq) → O2 (g) + 2H+ (aq)
चूँकि अभिक्रिया क्षारीय माध्यम में सम्पन्न होती है; अतः दोनों ओर OH– आयन जोड़ने पर –
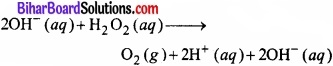
H+ तथा OH– आयन के संयोग से जल अणु बनने पर परिणामी समीकरण निम्नवत् होगी –
H2O2 (aq) + 20H– (aq) → O2 (g) + 2H2O (l)
पद 4.
अपचयन अर्द्ध-अभिक्रिया में सर्वप्रथम Cl परमाणुओं को सन्तुलित करते हैं –
Cl2O7 (g) → 2ClO2– (aq)
O परमाणुओं के सन्तुलन के लिए हम दाईं ओर तीन जल-अणु जोड़ते हैं –
Cl2O7 (g) → 2ClO2– (aq) + 3H2O (l)
H परमाणुओं के सन्तुलन के लिए हम 6H+ बाईं ओर जोड़ते हैं –
Cl2O7 (g) + 6H+ (aq) → 2ClO2– (aq) + 3H2O (l)
चूँकि अभिक्रिया क्षारीय माध्यम में सम्पन्न होती है; अत: 6H+ के लिए दोनों ओर 6OH+ जोड़ते हैं –
Cl2O7 (g) + 6H+ (aq) + 6OH– (aq) → 2ClO2– (aq) + 3H2O(l) + 6OH– (aq)
H+ तथा OH– के संयोग से जल अणु बनने पर परिणामी समीकरण निम्नवत् करते हैं –
Cl2O7 (g) + 3H2O (l) → 2ClO2–(aq) + 6OH– (aq)
पद 5.
इस पद में हम दोनों अर्द्ध-अभिक्रियाओं में आवेश का सन्तुलन निम्नवत् करते हैं –
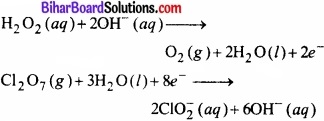
इलेक्ट्रॉनों की संख्या एकसमान करने के लिए ऑक्सीकरण अर्द्ध-अभिक्रिया की गुणा 4 से करते हैं।

पद 6.
उपर्युक्त दोनों अर्द्ध-अभिक्रियाओं को जोड़ने पर –

अन्तिम सत्यापन दर्शाता है कि समीकरण में दोनों ओर के परमाणुओं की संख्या तथा आवेश की दृष्टि से समीकरण सन्तुलित है।
ऑक्सीकरण संख्या विधि से समीकरण सन्तुलित करना –
पद 1.
अभिक्रिया का ढाँचा इस प्रकार है –

पद 2.
अभिक्रिया में Cl तथा O की ऑक्सीकरण संख्या लिखते हैं –

स्पष्ट है कि H2O2 अपचायक तथा Cl2O7 ऑक्सीकारक के रूप में कार्य करते हैं।
पद 3.
ऑक्सीकरण संख्या में होने वाली कमी तथा वृद्धि की गणना करते हैं तथा उन्हें एकसमान बनाते हैं –
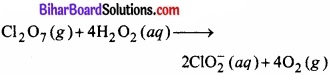
पद 4.
चूँकि अभिक्रिया क्षारीय माध्यम में हो रही है तथा दोनों ओर के आयनों का आवेश एकसमान नहीं है; अतः हम दो OH– आयन बाईं ओर जोड़ देते हैं –

H परमाणुओं के सन्तुलन के लिए दाईं ओर पाँच जल-अणु जोड़ते हैं।

![]()
प्रश्न 8.20
निम्नलिखित अभिक्रिया से आप कौन-सी सूचनाएँ प्राप्त कर सकते हैं –
(CN)2 (g) + 20H– (aq) → CN– (aq) + CNO– (aq) + H2O
उत्तर:
दी हुई अभिक्रिया से निम्नलिखित सूचनाएँ प्राप्त होती हैं –
(a) अभिक्रिया में क्षारीय माध्यम में सायनोजन (CN2) का वियोजन हो रहा हैं।
(b) (CN)2 तथा CN– दोनों प्रकृति में छद्म हैलोजन (pseudo halogen) हैं।
(c) यह एक असमानुपातन अभिक्रिया है। क्योंकि सायनोजन (CN)2 का CNO– में ऑक्सीकरण तथा CN– में अपचयन होता है।
प्रश्न 8.21
Mn3+ आयन विलयन में अस्थायी होता है तथा असमानुपातन द्वारा Mn2+, MNO2–, और H+ आयन देता है। इस अभिक्रिया के लिए सन्तुलित आयनिक समीकरण लिखिए।
उत्तर:
असमानुपातन अभिक्रिया का प्रमुख समीकरण हैं –
Mn3+ (aq) → Mn2+ (aq) + MnO2 (s) + H+ (aq)
पद 1.
दो अर्द्ध समीकरण निम्नवत हैं –
1. ऑक्सीकरण अर्द्ध-अभिक्रिया:
Mn3+ → MnO2
2. अपचयन अर्द्ध-अभिक्रिया:
Mn3+ → Mn2+
पद 2.
अर्द्ध-अभिक्रिया (i) में O परमाणुओं को संतुलित करने के लिए बाईं ओर 2 जल अणु जोड़ते हैं –
Mn3+ + 2H2O → MnO2
अर्द्ध समीकरण (ii) में H परमाणुओं को संतुलित करने के लिए 4H+ दाईं ओर जोड़ते हैं –
Mn3+ + 2H2O → MnO2 + 4H+
पद 3.
उपर्युक्त अर्द्ध समीकरणों में आवेशों का इलेक्ट्रॉनों द्वारा संतुलन निम्न प्रकार से करते हैं –

पद 4.
उपर्युक्त दोनों अर्द्ध समीकरणों को जोड़ने पर
2Mn3+ + 2H2O → MnO2 + Mn2+ + 4H+ जो अभीष्ट संतुलित समीकरण है।
![]()
प्रश्न 8.22
Cs, Ne, I तथा F में ऐसे तत्व की पहचान कीजिए, जो –
(क) केवल ऋणात्मक ऑक्सीकरण अवस्था प्रदर्शित करता है।
(ख) केवल धनात्मक ऑक्सीकरण अवस्था प्रदर्शित करता है।
(ग) ऋणात्मक तथा धनात्मक दोनों ऑक्सीकरण अवस्था प्रदर्शित करता है।
(घ) न ऋणात्मक और न ही धनात्मक ऑक्सीकरण अवस्था प्रदर्शित करता है।
उत्तर:
(क) F केवल ऋणात्मक ऑक्सीकरण अवस्था प्रदर्शित करता है।
(ख) Cs केवल धनात्मक ऑक्सीकरण अवस्था प्रदर्शित करता है।
(ग) I ऋणात्मक तथा धनात्मक दोनों ऑक्सीकरण अवस्था प्रदर्शित करता है।
(घ) Ne न ऋणात्मक और न ही धनात्मक ऑक्सीकरण अवस्था प्रदर्शित करता है।
प्रश्न 8.23
जल के शुद्धिकरण में क्लोरीन को प्रयोग में लाया जाता है। क्लोरीन की अधिकता हानिकारक होती है। सल्फर डाइऑक्ससाइड से अभिक्रिया करके इस अधिकता को दूर किया जाता है। जल में होने वाले इस अपचयोपचय परिवर्तन के लिए सन्तुलित समीकरण लिखिए।
उत्तर:
पद 1.
अभिक्रिया का ढांचा समीकरण निम्नवत् –
Cl2 + SO2 → Cl– + \(\mathrm{SO}_{4}^{2-}\)
पद 2.
दो अर्द्ध समीकरण इस प्रकार हैं –
1. ऑक्सीकरण अर्द्ध अभिक्रिया:
SO2 → \(\mathrm{SO}_{4}^{2-}\)
2. अपचयन अर्द्ध अभिक्रिया:
Cl2 → Cl–
पद 3.
अर्द्ध अभिक्रिया (i) में O परमाणुओं को संतुलित करने के लिए समीकरण में बाई ओर 2 जल अणु जोड़ते हैं –
SO2 + 2H2O → \(\mathrm{SO}_{4}^{2-}\) + 4H+
पद 4.
अभिक्रिया (ii) की संतुलित अर्द्ध-अभिक्रिया इस प्रकार है –
Cl2 → 2Cl–
पद 5.
उपर्युक्त दोनों अर्द्ध-अभिक्रियाओं में आवेशों का संतुलन इस प्रकार करते हैं –
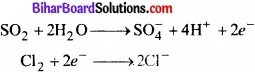
पद 6.
उपर्युक्त दोनों अर्द्ध अभिक्रियाओं के समीकरणों को जोड़ने पर
Cl2 + SO2 + 2H2O → 2Cl– + \(\mathrm{SO}_{4}^{2-}\) + 4H+ जो अभीष्ट संतुलित समीकरण है।
![]()
प्रश्न 8.24
इस पुस्तक में दी गई आवर्त सारणी की सहायता से निम्नलिखित प्रश्नों के उत्तर दीजिए –
(क) सम्भावित अधातुओं के नाम बताइए, जो असमानुपातन की अभिक्रिया प्रदर्शित कर सकती हों।
(ख) किन्ही तीन धातुओं के नाम बताइए, जो असमानुपातन अभिक्रिया प्रदर्शित कर सकती हों।
उत्तर:
(क) ऐसा अधातुएँ जो परिवर्ती ऑक्सीकरण संख्याओं में रह सकती हैं, असमानुपातन की अभिक्रिया कर सकती हैं। उदाहरणार्थ: फॉस्फोरस, क्लोरीन तथा सल्फर।
(ख) संक्रमण श्रेणी (d – बलॉक तत्व) से सम्बद्ध धातुएँ असमानुपातन अभिक्रियाएँ प्रदर्शित कर सकती हैं। उदाहरणार्थमैगनीज, आयरन तथा कॉपर।
प्रश्न 8.25
नाइट्रिक अम्ल निर्माण की ओस्टवाल्ड विधि के प्रथम पद में अमोनिया गैस के ऑक्सीजन गैस द्वारा ऑक्सीकरण से नाइट्रिक ऑक्साइड गैस तथा जलवाष्प बनती है। 10.0g अमोनिया तथा 20.00g ऑक्सीजन द्वारा नाइट्रिक ऑक्साइड की कितनी अधिकतम मात्रा प्राप्त हो सकती है?
उत्तर:
नाइट्रिक अम्ल की ओस्टवाल्ड विधि के प्रथम पद में अमोनिया गैस के ऑक्सीजन गैस द्वारा ऑक्सीजन से नाइट्रिक ऑक्साइड गैस तथा जलवाष्प का बनना निम्नलिखित अभिक्रिया के अनुसार है –

∵ 68g NH2 के लिए आवश्यक ऑक्सीजन = 160g
∴ 10g MH3 के लिए आवश्यक ऑक्सीजन = \(\frac{160}{68}\) × 10
= 23.6g
चूँकि ऑक्सीजन की उपलब्ध मात्रा 20g आवश्यक मात्रा 23.6g से कम है, अत: ऑक्सीजन सीमान्त अभिकर्मक है।
∵ 160g O2 से NO बनी है = 120g
∴ 20g O2 से NO बनेगी = \(\frac{120}{160}\) × 20
= 15g
प्रश्न 8.26
पाठ्य-पुस्तक की सारणी 8.1 में दिए गए मानक विभवों की सहायता से अनुमान लगाइए कि क्या इन अभिकारकों के बीच अभिक्रिया सम्भव है?
(क) Fe3+ तथा I– (aq)
(ख) Ag+ तथा Cu(s)
(ग) Fe3+ (aq) तथा Br– (aq)
(घ) Ag(s) तथा Fe3+ (aq)
(ङ) Br2 (aq) तथा Fe2+
उत्तर:

![]()
प्रश्न 8.27
निम्नलिखित में से प्रत्येक के विद्युत अपघटन से प्राप्त उत्पादों के नाम बताइए –
(क) सिल्वर इलेक्ट्रोड के साथ AgNO3 का जलीय विलयन
(ख) प्लैटिनम इलेक्ट्रोड के साथ AgNO3 का जलीय विलयन
(ग) प्लैटिनम इलेक्ट्रोड के साथ H2SO4 का तनु विलयन
(घ) प्लैटिनम इलेक्ट्रोड के साथ CuCl2 का जलीय विलयन।
उत्तर:
(क) सिल्वर इलेक्ट्रोड के साथ AgNO3 का जलीय विलयन देता है –

प्रश्न 8.28
निम्नलिखित धातुओं को उनके लवणों के विलयन में से विस्थापन की क्षमता के क्रम में लिखिए –
Al, Cu, Fe Mg तथा Zn
उत्तर:
Mg > AI > Zn > Fe > Cu
प्रश्न 8.29
नीचे दिए गए मानक इलेक्ट्रोड विभवों के आधार पर धातुओं को उनकी बढ़ती अपचायक क्षमता के क्रम में लिखिए –
K+ / K = -2.93 V, Ag+ / Ag = 0.80V,
Hg2+ / Hg = 0 79V,
Mg2+ / Mg = -2.37V, Cr3+ / Cr = -0.74V
उत्तर:
Ag < Hg < Cr < Mg < K
![]()
प्रश्न 8.30
उस गैल्वेनी सेल को चित्रित कीजिए, जिसमें निम्नलिखित अभिक्रिया होती है –
Zn(s) + 2Ag+ (aq) → Zn2+ (aq) + 2Ag(s) अब बताइए कि –
(क) कौन-सा इलेक्ट्रोड ऋण आवेशित है?
(ख) सेल में विद्युत-धारा के वाहक कौन हैं?
(ग) प्रत्येक इलेक्ट्रोड पर होने वाली अभिक्रियाएँ क्या है?
उत्तर:
Zn(s)|Zn2+(aq)||Ag+ (aq)|Ag(s)
(क) Zn इलेक्ट्रोड ऋण आवेशित है।
(ख) इलेक्ट्रॉन।
(ग)
ऐनोड पर: Zn → Zn2+ + 2e–
कैथोड पर: Ag+ + e– → Ag